Natriumtiosulfat är ett tiosulfatsalt av natrium.
| Natriumtiosulfat | |
  | |
| Systematiskt namn | Natriumtiosulfat |
|---|---|
| Övriga namn | Hyposulfitsoda, hypo |
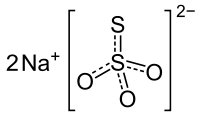
| Kemisk formel | Na2S2O3 |
| Molmassa | 158,108 g/mol |
| Utseende | Vita kristaller |
| CAS-nummer | 7772-98-7 |
| SMILES | [O-]S(=S)(=O)[O-].[Na+].[Na+] |
| Egenskaper | |
| Densitet | 1,667 g/cm³ |
| Löslighet (vatten) | 209 g/l (20 °C) |
| Smältpunkt | 48,3 °C |
| Kokpunkt | 100 °C (sönderfaller) |
| Faror | |
| NFPA 704 | |
| SI-enheter & STP används om ej annat angivits | |
Framställning
redigeraIndustriellt produceras natriumtiosulfat som en biprodukt vid tillverkningen av natriumsulfid. För laboratoriebruk kan saltet framställas genom att värma upp natriumsulfit tillsammans med svavel.
Egenskaper
redigeraNatriumtiosulfat kan neutralisera hypoklorit vilket är den aktiva ingrediensen i klorbaserade blekmedel.
Det kan också reagera med guld och bilda molekylen Na3[Au(S2O3)2].
Användning
redigera- Natriumtiosulfat kan användas som ett alternativ till natriumcyanid vid utvinning av guld. Nackdelen är att guldtiosulfat-jonerna inte kan filtreras fram med aktivt kol.
- Som fixerbad vid fotografisk framkallning. Ämnet går inom fotobranschen under namnet Hyposulfitsoda eller Hypo.
- För att kunna testa pH-värdet på blekmedel. Natriumtiosulfat neutraliserar hypoklorit-joner som annars skulle ha blekt bort färgerna av pH-indikatorn.
- Underkylt natriumtiosulfat kristalliserar sig med en exoterm reaktion vilket gör den användbar i till exempel kemiska handvärmare.
- Som motgift till cyanid. Natriumtiosulfat överför svavel-atomer till cyanid som övergår i ofarlig tiocyanat.
- Vid garvning av läder.
- För att neutralisera det jod-baserade konserveringsmedlet Lugols lösning. Lösningen konserverar till exempel celler i växtplanktonprover bruna, men tillsätter men natriumtiosulfat avfärgas provet och nya färgämnen kan tillsättas.
