Periodiska systemet
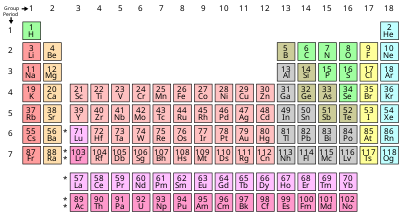
Periodiska systemet, även kallat grundämnenas ordning,[1] är en indelning av grundämnen och atomslag efter deras ökande atomnummer (antal protoner i kärnan), och även kemiska och fysikaliska egenskaper samt elektronkonfiguration i de yttre elektronskalen. Denna ordning visar periodiska trender, såsom grundämnen med liknande egenskaper i samma kolumn (grupp). Det finns även fyra rektangulära block med approximativt likartade kemiska egenskaper. Inom varje rad (period) återfinns i allmänhet metallerna på den vänstra sidan, medan icke-metallerna återfinns på den högra sidan.
Den första versionen av periodiska systemet ställdes upp av Dmitrij Mendelejev (1869), som var först med att publicera sina resultat, och Lothar Meyer. Allt eftersom nya grundämnen upptäckts och den teoretiska grundvalen för systemet fördjupats, har det modifierats och förfinats.
Ännu ej bekräftade grundämnen har tilldelats provisoriska namn, sammansatta av symboler för atomnumrets siffror inspirerade av räkneord från latin och grekiska, således: 0 = nil; 1 = un; 2 = bi; 3 = tri; 4 = quad; 5 = pent; 6 = hex; 7 = sept; 8 = okt; 9 = enn. Namnen avslutas med suffixet -ium. Exempel: 113 = ununtritium.
Ämnena 113 (borgruppen), 115 (kvävegruppen), 117 (halogen), 118 (ädelgas) var under många år förutspådda, men inte konstaterade. År 2014 framställdes emellertid dessa ämnen i laboratorier. Förklaringen till att ämnena inte har hittats i naturen är att de är radioaktiva med korta sönderfallstider. De sista luckorna i period 7 av Mendelejevs system har fyllts med de nyupptäckta ämnena.[2] De nya ämnenas fysikaliska och kemiska egenskaper är till stor del obekanta, men år 2016 fastslogs de officiella namnen till nihonium (113), moskovium (115), tenness (117) och oganesson (118).
Indelningar redigera
Grupper redigera
En grupp motsvarar en kolumn i en tabell över det periodiska systemet. I en del grupper har grundämnena mycket lika egenskaper och visar en tydlig trend för egenskaperna inom gruppen. Dessa grupper brukar tilldelas triviala (osystematiska) namn, som exempelvis alkalimetaller, alkaliska jordmetaller, halogener och ädelgaser. Vissa andra grupper i det periodiska systemet påvisar färre likheter och/eller kolumnvisa trender (exempelvis grupperna 4 och 5) och dessa har därför inte tilldelats triviala namn utan benämns endast utifrån gruppnummer.
Perioder redigera
En period motsvarar en rad i det periodiska systemets tabell. Även om grupper är det vanligaste sättet att klassificera grundämnen, finns det vissa områden där de radvisa trenderna och likheterna är viktigare än de kolumnvisa grupptrenderna. Detta gäller bland annat d-blocket liksom f-blocket där lantanoiderna och aktinoiderna bildar två viktiga radvisa serier av grundämnen. Lantanoiderna och aktinoiderna placeras under varandra utanför den övriga delen av det periodiska systemets tabell av det praktiska skälet att tabellbredden därmed minskas avsevärt.[3]
Block redigera
Ett block är en familj av angränsande grupper. Dessa områden får sina namn från atomernas elektronskal. Det finns fyra block: s-, p-, d- och f-blocket.
Övriga redigera
Grundämnena kan även delas in och grupperas på andra sätt. Några sådana indelningar som ofta ritas in det periodiska systemet är övergångsmetaller och metalloider. Det finns även mer inofficiella indelningar såsom platinagruppen och ädelmetallerna.
Historik redigera
De tidigaste försöken att ordna och gruppera grundämnena gjordes utan någon kunskap om atomernas uppbyggnad. Den tyske kemisten Johann Wolfgang Döbereiner försökte hitta samband mellan olika ämnens atomvikt och deras kemiska egenskaper och fann på 1820-talet flera grupper av tre likartade ämnen, där ett av ämnena kemiskt var en blandning av de båda andra och hade en atomvikt som låg mitt emellan de övrigas. Han kallade dessa för triader.
Newlands tabell redigera
Under flera decennier betraktas Döbereiners upptäckt som en oväsentlig kuriositet, vad vetenskapshistorikern Stephen Toulmin kallar för ett "naket faktum", men när nya och riktigare uppgifter om olika ämnens atomvikter blev kända under 1860-talet, intresserade sig olika forskare för nya samband mellan atomvikter och kemiska egenskaper. År 1866 uppställde den brittiske kemisten John Newlands en tabell med 62 av de då 63 kända grundämnena, ordnade efter stigande atomvikt. Tabellen visade att ämnen med liknande egenskaper återkom med en periodicitet av 7 eller 14 ämnen (ädelgaserna var ännu inte upptäckta), ungefär som oktaver i musiken. Andra tidiga versioner av systemet presenterades av Alexandre-Émile Béguyer de Chancourtois och William Odland.
Mendelejevs och Meyers system redigera
Slutligen sammanställde 1869 ryssen Dmitrij Mendelejev och tysken Lothar Meyer oberoende av varandra tabeller med horisontella perioder och vertikala grupper, på samma sätt som vi nu är vana att visa systemet. Mendelejev publicerade sitt arbete samma år medan Meyer publicerade sina resultat först 1870. Mendelejevs tabell hade luckor för ytterligare 31 ämnen, där inga av de då kända ämnena passade in. Hans idéer fick därför stor uppmärksamhet när det 1875 upptäckta ämnet gallium passade in i en av dessa luckor. När även ämnena skandium, som upptäcktes 1879, och germanium, upptäckt 1886, passade in i mönstret fick systemet stor acceptans bland övriga vetenskapsmän.
Efter Mendelejev redigera
1905 ritade schweizaren Alfred Werner upp det 32 kolumner stora periodiska system vi har idag och löste därmed problem som fanns i Meyers och Mendelejevs system från 1860-talet. Det periodiska systemets utseende fick dock sin förklaring först senare, efter att Rutherford 1911 presenterat sin modell av atomen som en liten positivt laddad kärna omgiven av elektroner och Bohr 1913 förklarat elektronernas energinivåer med sin kvantmekaniska atommodell.[4]
Det äldre systemet med 8 kolumner / grupper användes ibland efter 1905. Under 1920-talet, efter Mendelejev och Meyer, har systemet tydliggjorts. Fler och fler luckor i systemet har fortsatt att fyllas, allt eftersom ytterligare grundämnen har upptäckts. Idag är alla 7 perioder kompletta. Om fler grundämnen upptäcks, kommer de att finnas i period 8 och uppåt.
Andra sätt att ordna grundämnen redigera
En begränsning med periodiska systemet är att det inte skiljer mellan isotoper av samma element (det vill säga element med samma antal protoner, men olika antal neutroner), eftersom dessa i regel inte har någon stor skillnad i kemiska egenskaper (dock uppvisar kemiska föreningar med olika isotoper mätbara skillnader i kemiska egenskaper, såsom tungt vattens skillnader gentemot vanligt vatten, eller i reaktioners kinetik som är noterbar i särskilt organiska reaktioner). Isotoper har däremot mycket uppenbart olika egenskaper med avseende på stabilitet och radioaktivitet. Ett alternativt sätt att tabellera grundämnen, som skiljer på olika isotoper, är en nuklidkarta (alternativt isotoptabell). En nuklidkarta ger bättre förståelse för olika isotopers karaktär än det periodiska systemet, men ger å andra sidan inte samma överblick av de kemiska egenskaperna.
Se även redigera
Källor redigera
- ^ Tweed, Matt (2003). Kemins värld: en titt på periodiska systemet. Svenska förlaget. ISBN 9789177386469
- ^ Nationalencyklopedins årsbok nr 40 2015, Nationalencyklopedin AB, Malmö 2016, ISBN 978-91-7513-063-7
- ^ ”Periodiska systemet”. Nationalencyklopedin. http://www.ne.se/lang/periodiska-systemet. Läst 16 december 2009.
- ^ Pais, Abraham (1988). ”Atomic structure and spectral lines”. Inward Bound – Of Matter and Forces in the Physical World. Oxford University Press. ISBN 978-0-19-851997-3
Externa länkar redigera
- Wikimedia Commons har media som rör Periodiska systemet.