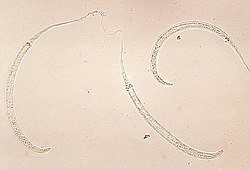
Guineamask (Dracunculus medinensis), även medinamask[1], är en rundmask som parasiterar människor och vissa däggdjur. Smittan överförs genom att värden dricker vatten med hoppkräftor, som är guineamaskens mellanvärd. Via mellanvärden förs ett larvstadium in i slutvärden.[2]
| Guineamask | |
 | |
| Systematik | |
|---|---|
| Domän | Eukaryoter Eukaryota |
| Rike | Djurriket Animalia |
| Stam | Rundmaskar Nematoda |
| Klass | Chromadorea |
| Ordning | Rhabditida |
| Överfamilj | Dracunculoidea |
| Familj | Dracunculidae |
| Släkte | Dracunculus |
| Art | Guineamask D. medinensis |
| Vetenskapligt namn | |
| § Dracunculus medinensis | |
| Auktor | Linné, 1758 |
| Synonymer | |
| |
| Hitta fler artiklar om djur med | |
Både hon- och hanlarver använder hoppkräftor som vektor och för att utvecklas. De parar sig i buken på slutvärden. Efter parningen dör hanen medan honan tar sig genom tarmväggen för att leva i bindväven. Honan producerar miljontals ägg. När larverna är redo att frisätts från honan bildas en blåsa i värden. När blåsan kommer i kontakt med vatten spricker den och larverna frisätts i vattnet.[3] Honan kan bli cirka 1 meter lång[4] och cirka 2 mm i diameter,[5] medan hanen bara blir upp till 4 cm lång.[4]
Djuret tillhör fylumet rundmaskar (Nematoda)[3] och dess vetenskapliga namn är Dracunculus medinensis, vilket är latin där förledet betyder ”lidande av små drakar”.[6] Parasiten har plågat människan under lång tid och har bland annat återfunnits i egyptiska mumier.[6] Idag arbetar Världshälsoorganisationen (WHO) med att utrota arten.[2]
Morfologi
redigeraGuineamaskens kropp är cylindrisk, slät och mjölkvit i färgen. Huvudet har en kitinsköld på vilken det finns sex papiller, vilket är en sorts sensoriska strukturer. Vuxna har också sex labiala papiller och åtta externa papiller vid sidan om läppen.
Hanar och honor uppvisar könsdimorfism, vilket innebär att de visuellt går att särskilja åt.[7]
Honan är den längsta av alla kända nematoder som parasiterar människor. Den vuxna honan är en smal, lång, mjölkaktig vit mask som mäter 60-120 cm (ungefär en meter) i längd och 1,5–1,7 mm i tjocklek. Hona har en trubbig främre ände och en avsmalnande bakre ände. Honor har två livmödrar (uteri) som fylls med embryon; alla andra organ inklusive matsmältningskanalen tillbakabildas. Ungefär 3 miljoner embryon kan finnas i livmodern hos en befruktad hona. Masken är vivipar, vilket innebär att den föder levande larver.[7]
Hanen är mycket mindre än honan, med en längd på 12–30 mm och en bredd på 0,4 mm (se figur 2). Den bakre änden av hanen är konisk, där det finns 10 par könspapiller. Hanar har en spicula, ett utskott av olika längd, och ett gubernaculum som hjälper dem att öppna honors vulva och föra in spermier under kopuleringen.[7]
Livscykel
redigeraParasiten har en livscykel där den nyttjar vattenlevande hoppkräftor som mellanvärd, fiskar och grodor som transport- och mellanvärd och människan hundar och katter som slutvärd.[4][6] Parasiten använder mellanvärden för näringstillgång och tillväxt och inne i mellanvärden genomgår den två larvstadier. Slutstadiet kallas L3 och infaller efter två till 14 dagar.[4] Då är larverna infekterande och redo att byta värd. Genom konsumtion av orenat eller ofiltrerat vatten där det förekommer larvbärande hoppkräftor riskerar människor att bli smittade.[5] Larverna frigörs när hoppkräftorna dör och löses upp av magsyran. Larverna vandrar genom tarmväggen och utvecklas i slutvärden till fullbildade, könsmogna individer. De parar sig med varandra efter ca 100 dagar i värden.[9] Hanen dör efter parningen, inkapslad i vävnaden medan honan lever vidare för att sörja för utvecklingen av äggen. Honan förflyttar sig till bindväven i extremiteterna.[9] Där produceras miljontals ägg som honan bär på tills de har blivit larver som är redo att frisättas.[4] Larverna frisätts genom en blåsa som värden upplever som en smärtsam brännande känsla. Blåsan brukar vanligtvis bildas i fötter och underben, sällan i andra delar av kroppen.[10] För att lindra smärtan är det vanligt att värden placerar kroppsdelen under vatten där blåsan spricker och larverna frisätts i vattnet och cykeln börjar om.[4] Honan initierar bildningen av blåsan, för att frisätta larverna, ungefär ett år efter infektionen.[10]
Nyupptäckta smittvägar
redigeraD. medinensis smittar människan, men även hundar och katter i utsatta områden har konstaterats bära på parasiten. Tidigare antogs att överföringen av parasiten via hoppkräftor var enda vägen för guineamasken att ta sig in i människokroppen. När observationer av infekterade domesticerade hundar ökade år 2012, senare även katter, väcktes tankarna om att andra parateniska (infekterade) mellanvärdar kunde vara involverade i livscykeln. Den nya hypotesen är att fiskar, grodor och andra vattenlevande djur kan fungera som mellanvärdar och att människor, hundar och katter blir infekterade genom att äta underkokt, eller rått kött från dessa vattenlevande djur. Studier tyder vidare på att fiskar fungerar som transportvärdar snarare än en paratenisk värd. Mer forskning krävs för att fastställa de vattenlevande djurens roll. En undersökning visar att hundar sväljer hoppkräftor genom den klassiska smittvägen. Men antalet larver som de får i sig när de dricker sjö eller flodvatten var lägre än förväntat utifrån det antal maskar som påträffas i infekterade hundar. Det stödjer hypotesen om alternativa överföringsvägar.[11]
Värd-parasitrelation
redigeraVärden är som regel omedveten om parasitinfektionen fram tills att honmasken framträder genom huden. För att undgå upptäckt av värdens immunförsvar maskerar sig guineamasken med en hinna som efterliknar de mänskliga proteinerna albumin och immunoglobulin (isotyp IgG). Hinnan förhindrar immunförsvarets antikroppar från att binda sig till parasitens yta av antigener och på så sätt undviker guineamasken att parasit-inducerade inflammatoriska processer aktiveras.[12] Analyser har också visat att guineamask producerar den aktiva metaboliten morfin 6-glukuronid (M6G) som hämmar smärtsignaleringen hos värden.[13] Morfin har också förmågan att hämma immunförsvaret reaktionsförmåga vilket lett till en hypotes om att morfinsekretion från parasiten sker i detta syfte. Sådan sekretion har återfunnits i flera parasiter, framförallt inom nematodstammen. Det är dock okänt om morfinsekretionen sker aktivt av parasiten i värden eller om det läcker ut under tillväxtperioden.[14]
Sjukdom
redigeraDracontiasis, Guineamaskinfektion, märks då larverna är redo att frisättas från honan, vilket sker ungefär ett år efter det att smittat vatten har konsumerats.[5] En blåsa bildas på huden och parasiten orsakar en brännande känsla, vilket ofta leder till att värden försöker lindra smärtan, ofta genom att svalka med vatten. I vattnet spricker blåsan och miljontals larver av första larvstadiet (L1) tar sig ut i vattnet. Larverna äts därefter av hoppkräftor. Den kraftiga smärtan åtföljs av kräkningar, feber, illamående,[9] diarréer och yrsel.[4] Det kan ta några veckor, till några månader, för honmasken att ta sig ut vilket leder till ett hälsotillstånd som gör värden sängliggande.[15] Området där parasiten tar sig ut blir ofta fyllt av blåsor och sår. Den intensiva klådan leder ofta till att infektioner uppstår i området. Eftersom masken ofta kommer ut ur foten eller ur benet kan detta leda till att värden får svårt att gå. Under tiden som masken framträder är det viktigt att den inte går av eftersom detta kan leda till allvarliga allergiska reaktioner. Tillståndet leder dock sällan till döden.[9] Vanligtvis brukar infekterade människor ha en till tre maskar, men så många som 40 stycken har påträffats hos en och samma individ.[6]
Behandling
redigeraVanligtvis rullar man upp masken centimeter för centimeter på en pinne. Processen är väldigt smärtsam och kan ta veckor − ibland månader. Lyckas man inte med upprullningen kan man avlägsna masken med kirurgi om tillgång till läkare finns.[6] Det finns ingen medicin eller vaccin utan man måste arbeta förebyggande genom att rena dricksvatten.[2]
Utbredning
redigeraParasiten har främst hittats i utvecklingsländer, söder om Sahara. Guineamaskens globala utbredning har sedan år 1986 minskat från 20 länder till endast 9 stycken år 2006.[6] År 2019 rapporterades totalt 53 fall av människor som infekterats av guineamasken i Tchad, Sydsudan, Angola och Kamerun, varav 47 av dessa fall rapporterades från Tchad. Vidare rapporterades inga fall av infekterade människor i Mali eller Etiopien. Totalt 1973 infekterade hundar, katter och babianer rapporterades i Tchad, 9 i Mali, 8 i Etiopien och 1 i Angola. Inga infekterade djur rapporterades i Sydsudan eller Kamerun under 2019.[16]
Utrotning
redigeraGenom olika hälsofrämjande insatser har antalet infekterade av guineamask under de senaste 50 åren minskat radikalt. Från cirka 50 miljoner fall 1950 till cirka 1 800 fall år 2010[9], endast 25 fall år 2016[16] och 53 fall år 2019.[17]1980 startades en utrotningskampanj av Centers for disease control and prevention (CDC) vilket sedan även blev ett mål för United Nations International Drinking-Water Supply and Sanitation Decade 1981–1990. Filter för rening av vatten och ekonomiskt stöd för byggandet av nya brunnar delas ut till utsatta områden. Åtgärder som WHO nu tar till, är kartläggning av byar och kommunikativ övervakning i varje smittad by, alla fall ska rapporteras in. Vid nya sjukdomsfall får den drabbade såret rengjort och ges rådet att undvika vattenhål.[18] Regelbunden rapportering och tillgång till renat vatten, filtrering, kontroll av vattenhål och genom att övervaka utrotningen av parasiten i land för land, är en del av åtgärderna.[2]
År 1986 startades programmet "Guinea Worm Eradication Program" (GWEP) som leddes av The Carter Center. Programmet var tänk att pågå till och med 1991 men målet för utrotningen flyttades fram till 2009, 2015, 2020 och därefter till 2030.[19] För att skynda på arbetet anslöt sig även World Heath Assembly år 2011, vilka uppmanade alla medlemsstater genom WHA 64.16 att intensifiera övervakning av spridning samt effektivisera åtgärder innefattande vektorkontroll, hälsoundervisning och filtrering av dricksvatten genom tyg eller rör.[20]
Nya Bekämpningsåtgärder
redigeraFördröjningen av utrotningen har främst berott på att andra värdar än människan upptäckts. Forskarna har länge vetat att hundar och andra däggdjur kan vara värd för guineamasken men antagit att det rört sig om en annan art i släktet Dracunculus. En annan tolkning var att observationerna representerade undantag med överföringar från människa till hund och andra däggdjur. Infekterade hundar har främst observerats nära fiskebyar under fiskets högsäsong. Det leder till hypotesen att hundarna smittas via restprodukter från fisket. De nya rekommendationerna innebär att restprodukter från fisket ska grävas ned i drabbade områden. Vidare ska hundar, som visar tecken på infektion, hållas kopplade när larverna sprids i vattnet.[21] Kravet för att WHO ska deklarera ett land fritt från D. medinensis är att landet inte haft något fall av infekterade människor eller djur i >3 år. År 2018 rapporterades sammanlagt 28 infekterade människor i Angola, Tchad och Sydsudan och sammanlagt 1,102 infekterade djur rapporterades i Tchad, Ethiopia och Mali under samma år.[22] Det finns inga bevis för att guineamask kan föras över från ryggradsdjur till människa men att så pass många djur blir smittade försvårar utrotningsarbetet eftersom hundar och andra däggdjur återinför larverna till vattendragen.[19]
Referenser
redigera- ^ Nationalencyklopedin Höganäs 1994
- ^ [a b c d] WHO (2019) Dracunculiasis eradication: “on the threshold of a historic achievement” https://www.who.int/news-room/detail/26-09-2019-dracunculiasis-eradication-on-the-threshold-of-a-historic-achievement+>,
- ^ [a b] Bush, A.O. Fernandez, J.C. Esch, G.W. Seed, J.R (2001) Parasitism: The Diversity and Ecology of Animal Parasites, Cambridge University Press, sid. 186
- ^ [a b c d e f g] Nnaemeka C. Iriemenam, Wellington A. Oyibo and Adetayo F. Fagbenro-Beyioku (2008) Dracunculiasis-the saddle is virtually ended, Parasitology Resarch, vol. 102, sid. 343–347, DOI:10.1007/s00436-007-0828-9
- ^ [a b c] Glenshaw MT, Roy S, Ruiz-Tiben E, Downs P, Williamson J, Eberhard M. (2009) Guinea Worm Disease Outcomes in Ghana: Determinants of Broken Worms, The American Journal of Tropical Medicine and Hygiene vol. 81, nr.2, sid. 305–312
- ^ [a b c d e f g] Michele Barry, M.D. (2007) The Tail End of Guinea Worm - Global Eradication without a Drug or a Vaccine, The New England Journal of Medicine, vol. 356 sid. 2561–2564
- ^ [a b c] Dr. Ranjana Saxena Dyal Singh College, University of Delhi. Morphology, Life Cycle, Pathogenicity and Prophylaxis of Dracunculus medinensis Paper No.08 Biology of Parasitism, MHRD Govt. Of India). http://epgp.inflibnet.ac.in/epgpdata/uploads/epgp_content/zoology/08._biology_of_parasitism/27._morphology,_life_cycle,_pathogenicity_and_prophylaxis_of_dracunculus/et/7839_et_et.pdf
- ^ DPDx (2015) Life cycle image and information. Centers for Disease Control and Prevention. https://www.cdc.gov/parasites/guineaworm/biology.html
- ^ [a b c d e] WHO (2011) about guineaworm disease, <www.who.int>,
- ^ [a b] Cairncross S., Muller R. och Muller Z. N.2 (2002) Dracunculiasis (Guinea Worm Disease) and the Eradication Initiative. Department of Infectious and Tropical Diseases, London School of Hygiene and Tropical Medicine, London WC1E 7HT, United Kingdom,1 Department of Control, Prevention and Eradication of Communicable Diseases, World Health Organization, Geneva, Switzerland. DOI: 10.1128/CMR.15.2.223–246.2002 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC118073/pdf/0017.pdf
- ^ Eberhard, M. L., Ruiz-Tiben, E., Hopkins, D. R., Farrell, C., Toe, F., Weiss, A., Withers Jr., P. C., Jenks, M. H., Thiele E. A., Cotton, J. A., Hance, Z., Holroyd, N., Cama, V. A., Tahir, M. A. & Mounda T. 2014. The Peculiar Epidemiology of Dracunculiasis in Chad. The American Journal of Tropical Medicine and Hygiene 90(1): 61-70. doi: https://doi.org/10.4269/ajtmh.13-0554.
- ^ Bloch, P., Lund, M., Vennervals, B. J. & Simonsen, P. E. (1999) Human serum albumin and immunoglobulin on Dracunculus medinensis. Acta Tropica, 73(2), ss. 135-141. https://doi.org/10.1016/S0001-706X(99)00024-8
- ^ Zhu, W., Baggerman, G., Evan Secor, W., Casares, F., Pryor, S. C., Fricchione, G. L., Ruiz-Tiben, E., Eberhard, M. L. Bimi, L. & Stefano, G. B. (2013) Dracunculus medinensis and Ashistosoma mansoni contain opiate alkaloids. Annals of Tropical Medicine & Parasitology, 96(2), ss. 309-316. https://doi.org/10.1179/000349802125000808
- ^ Zhu, W,. Pryor, Stephen C., Putnam, J., Cadet, P & Stefano, G. B. (2004) Opiate Alkaloids and Nitric Oxide Production in the Nematode Ascaris suum. The Journal of Parasitology, 90(1), ss.15-22
- ^ WHO (2011) The disease and it's transmission, <www.who.int>,
- ^ [a b] The Carter Center, 2018 ”Eradication of Guinea worm disease - casa statement”. . https://www.cartercenter.org/resources/pdfs/health/guinea_worm/gw-case-statement.pdf
- ^ The Carter Center (2020) ”53 Cases of Guinea Worm Reported in 2019”. https://www.cartercenter.org/news/pr/2020/guinea-worm-worldwide-cases-jan2020.html
- ^ WHO (2011) Community-Based surveillance and case containment activities, <www.who.int>
- ^ [a b] The Lancet Infectious Diseases (November 2019). ”Dracunculiasis—a case study for infection eradication”. The Lancet 19: sid. 1149. DOI: https://doi-org.proxy.lnu.se/10.1016/S1473-3099(19)30488-8 https://www-sciencedirect-com.proxy.lnu.se/science/article/pii/S1473309919304888
- ^ ”Eradicating dracunculiasis”. World Health Organization. https://www.who.int/activities/eradicating-dracunculiasis
- ^ Ewen Callaway (5 januari 2016). ”Dogs thwart effort to eradicate Guinea worm - Epidemic in dogs complicates push to wipe out parasite.”. Nature 529: sid. 10-11. DOI: 10.1038/529010a
- ^ Donald R. Hopkins, Adam J. Weiss, Sharon L. Roy, James Zingeser, Sarah Anne J. Guagliardo (1 november 2019).”Progress Toward Global Eradication of Dracunculiasis — January 2018–June 2019”. MMWR Morbidity and Mortality Weekly Report 68: sid. 979–984. DOI: http://dx.doi.org/10.15585/mmwr.mm6847a3 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6822808/